Перед изучением этого раздела рекомендую прочитать следующую статью:
Классификация неорганических веществ
Основания – сложные вещества, которые состоят из катиона металла Ме+ (или металлоподобного катиона, например, иона аммония NH4+) и гидроксид-аниона ОН—.
По растворимости в воде основания делят на растворимые (щелочи) и нерастворимые основания. Также есть неустойчивые основания, которые самопроизвольно разлагаются.
Получение оснований
1. Взаимодействие основных оксидов с водой. При этом с водой реагируют в обычных условиях только те оксиды, которым соответствует растворимое основание (щелочь). Т.е. таким способом можно получить только щёлочи:
основный оксид + вода = основание
Например, оксид натрия в воде образует гидроксид натрия (едкий натр):
Na2O + H2O → 2NaOH
При этом оксид меди (II) с водой не реагирует:
CuO + H2O ≠
2. Взаимодействие металлов с водой. При этом с водой реагируют в обычных условиях только щелочные металлы (литий, натрий, калий. рубидий, цезий), кальций, стронций и барий. При этом протекает окислительно-восстановительная реакция, окислителем выступает водород, восстановителем является металл.
металл + вода = щёлочь + водород
Например, калий реагирует с водой очень бурно:
2K0 + 2H2+O → 2K+OH + H20
3. Электролиз растворов некоторых солей щелочных металлов. Как правило, для получения щелочей электролизу подвергают растворы солей, образованных щелочными или щелочноземельными металлами и бескилородными кислотами (кроме плавиковой) – хлоридами, бромидами, сульфидами и др. Более подробно этот вопрос рассмотрен в статье Электролиз.
Например, электролиз хлорида натрия:
2NaCl + 2H2O → 2NaOH + H2↑ + Cl2↑
4. Основания образуются при взаимодействии других щелочей с солями. При этом взаимодействуют только растворимые вещества, а в продуктах должна образоваться нерастворимая соль, либо нерастворимое основание:
щелочь + соль1 = соль2↓ + щелочь
либо
щелочь + соль1 = соль2↓ + щелочь
Например: карбонат калия реагирует в растворе с гидроксидом кальция:
K2CO3 + Ca(OH)2 → CaCO3↓ + 2KOH
Например: хлорид меди (II) взаимодействет в растворе с гидроксидом натрия. При этом выпадает голубой осадок гидроксида меди (II):
CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl
Химические свойства нерастворимых оснований
1. Нерастворимые основания взаимодействуют с сильными кислотами и их оксидами (и некоторыми средними кислотами). При этом образуются соль и вода.
нерастворимое основание + кислота = соль + вода
нерастворимое основание + кислотный оксид = соль + вода
Например, гидроксид меди (II) взаимодействует с сильной соляной кислотой:
Cu(OH)2 + 2HCl = CuCl2 + 2H2O
При этом гидроксид меди (II) не взаимодействует с кислотным оксидом слабой угольной кислоты – углекислым газом:
Cu(OH)2 + CO2 ≠
2. Нерастворимые основания разлагаются при нагревании на оксид и воду.
Например, гидроксид железа (III) разлагается на оксид железа (III) и воду при прокаливании:
2Fe(OH)3 = Fe2O3 + 3H2O
3. Нерастворимые основания не взаимодействуют с амфотерными оксидами и гидроксидами.
нерастворимое оснвоание + амфотерный оксид ≠
нерастворимое основание + амфотерный гидроксид ≠
4. Некоторые нерастворимые основания могут выступать в качестве восстановителей. Восстановителями являются основания, образованные металлами с минимальной или промежуточной степенью окисления, которые могут повысить свою степень окисления (гидроксид железа (II), гидроксид хрома (II) и др.).
Например, гидроксид железа (II) можно окислить кислородом воздуха в присутствии воды до гидроксида железа (III):
4Fe+2(OH)2 + O20 + 2H2O → 4Fe+3(O-2H)3
Химические свойства щелочей
1. Щёлочи взаимодействуют с любыми кислотами – и сильными, и слабыми. При этом образуются средняя соль и вода. Эти реакции называются реакциями нейтрализации. Возможно и образование кислой соли, если кислота многоосновная, при определенном соотношении реагентов, либо в избытке кислоты. В избытке щёлочи образуется средняя соль и вода:
щёлочь(избыток)+ кислота = средняя соль + вода
щёлочь + многоосновная кислота(избыток) = кислая соль + вода
Например, гидроксид натрия при взаимодействии с трёхосновной фосфорной кислотой может образовывать 3 типа солей: дигидрофосфаты, фосфаты или гидрофосфаты.
При этом дигидрофосфаты образуются в избытке кислоты, либо при мольном соотношении (соотношении количеств веществ) реагентов 1:1.
NaOH + H3PO4 → NaH2PO4 + H2O
При мольном соотношении количества щелочи и кислоты 2:1 образуются гидрофосфаты:
2NaOH + H3PO4 → Na2HPO4 + 2H2O
В избытке щелочи, либо при мольном соотношении количества щелочи и кислоты 3:1 образуется фосфат щелочного металла.
3NaOH + H3PO4 → Na3PO4 + 3H2O
2. Щёлочи взаимодействуют с амфотерными оксидами и гидроксидами. При этом в расплаве образуются обычные соли, а в растворе – комплексные соли.
щёлочь (расплав) + амфотерный оксид = средняя соль + вода
щёлочь (расплав) + амфотерный гидроксид = средняя соль + вода
щёлочь (раствор) + амфотерный оксид = комплексная соль
щёлочь (раствор) + амфотерный гидроксид = комплексная соль
Например, при взаимодействии гидроксида алюминия с гидроксидом натрия в расплаве образуется алюминат натрия. Более кислотный гидроксид образует кислотный остаток:
NaOH + Al(OH)3 = NaAlO2 + 2H2O
А в растворе образуется комплексная соль:
NaOH + Al(OH)3 = Na[Al(OH)4]
Обратите внимание, как составляется формула комплексной соли: сначала мы выбираем центральный атом (как правило, это металл из амфотерного гидроксида). Затем дописываем к нему лиганды — в нашем случае это гидроксид-ионы. Число лигандов, как правило, в 2 раза больше, чем степень окисления центрального атома. Но комплекс алюминия — исключение, у него число лигандов чаще всего равно 4. Заключаем полученный фрагмент в квадртаные скобки — это комплексный ион. Определяем его заряд и снаружи дописываем нужное количество катионов или анионов.
3. Щёлочи взаимодействуют с кислотными оксидами. При этом возможно образование кислой или средней соли, в зависимости от мольного соотношения щёлочи и кислотного оксида. В избытке щёлочи образуется средняя соль, а в избытке кислотного оксида образуется кислая соль:
щёлочь(избыток) + кислотный оксид = средняя соль + вода
либо:
щёлочь + кислотный оксид(избыток) = кислая соль
Например, при взаимодействии избытка гидроксида натрия с углекислым газом образуется карбонат натрия и вода:
2NaOH + CO2 = Na2CO3 + H2O
А при взаимодействии избытка углекислого газа с гидроксидом натрия образуется только гидрокарбонат натрия:
2NaOH + CO2 = NaHCO3
4. Щёлочи взаимодействуют с солями. Щёлочи реагируют только с растворимыми солями в растворе, при условии, что в продуктах образуется газ или осадок. Такие реакции протекают по механизму ионного обмена.
щёлочь + растворимая соль = соль + соответствующий гидроксид
Щёлочи взаимодействуют с растворами солей металлов, которым соответствуют нерастворимые или неустойчивые гидроксиды.
Например, гидроксид натрия взаимодействует с сульфатом меди в растворе:
Cu2+SO42- + 2Na+OH— = Cu2+(OH)2—↓ + Na2+SO42-
Также щёлочи взаимодействуют с растворами солей аммония.
Например, гидроксид калия взаимодействует с раствором нитрата аммония:
NH4+NO3— + K+OH— = K+NO3— + NH3↑ + H2O
! При взаимодействии солей амфотерных металлов с избытком щёлочи образуется комплексная соль !
Давайте рассмотрим этот вопрос подробнее. Если соль, образованная металлом, которому соответствует амфотерный гидроксид, взаимодействует с небольшим количеством щёлочи, то протекает обычная обменная реакция, и в осадок выпадает гидроксид этого металла.
Например, избыток сульфата цинка реагирует в растворе с гидроксидом калия:
ZnSO4 + 2KOH = Zn(OH)2↓ + K2SO4
Однако, в данной реакции образуется не основание, а амфотерный гидроксид. А, как мы уже указывали выше, амфотерные гидроксиды растворяются в избытке щелочей с образованием комплексных солей. Таким образом, при взаимодействии сульфата цинка с избытком раствора щёлочи образуется комплексная соль, осадок не выпадает:
ZnSO4 + 4KOH = K2[Zn(OH)4] + K2SO4
Таким образом, получаем 2 схемы взаимодействия солей металлов, которым соответствуют амфотерные гидроксиды, с щелочами:
соль амф.металла(избыток) + щёлочь = амфотерный гидроксид↓ + соль
соль амф.металла + щёлочь(избыток) = комплексная соль + соль
5. Щёлочи взаимодействуют с кислыми солями. При этом образуются средние соли, либо менее кислые соли.
кислая соль + щёлочь = средняя соль + вода
Например, гидросульфит калия реагирует с гидроксидом калия с образованием сульфита калия и воды:
KHSO3 + KOH = K2SO3 + H2O
Свойства кислых солей очень удобно определять, разбивая мысленно кислую соль на 2 вещества — кислоту и соль. Например, гидрокарбонта натрия NaHCO3 мы разбиваем на уольную кислоту H2CO3 и карбонат натрия Na2CO3. Свойства гидрокарбоната в значительной степени определяются свойствами угольной кислоты и свойствами карбоната натрия.
6. Щёлочи взаимодействуют с металлами в растворе и расплаве. При этом протекает окислительно-восстановительная реакция, в растворе образуется комплексная соль и водород, в расплаве — средняя соль и водород.
! Обратите внимание! С щелочами в растворе реагируют только те металлы, у которых оксид с минимальной положительной степенью окисления металла амфотерный!
Например, железо не реагирует с раствором щёлочи, оксид железа (II) — основный. А алюминий растворяется в водном растворе щелочи, оксид алюминия — амфотерный:
2Al + 2NaOH + 6H2+O = 2Na[Al+3(OH)4] + 3H20
7. Щёлочи взаимодействуют с неметалами. При этом протекают окислительно-восстановительные реакции. Как правило, неметаллы диспропорционируют в щелочах. Не реагируют с щелочами кислород, водород, азот, углерод и инертные газы (гелий, неон, аргон и др.):
NaOH +О2 ≠
NaOH +N2 ≠
NaOH +C ≠
Сера, хлор, бром, йод, фосфор и другие неметаллы диспропорционируют в щелочах (т.е. самоокисляются-самовосстанавливаются).
Например, хлор при взаимодействии с холодной щелочью переходит в степени окисления -1 и +1:
2NaOH +Cl20 = NaCl— + NaOCl+ + H2O
Хлор при взаимодействии с горячей щелочью переходит в степени окисления -1 и +5:
6NaOH +Cl20 = 5NaCl— + NaCl+5O3 + 3H2O
Кремний окисляется щелочами до степени окисления +4.
Например, в растворе:
2NaOH + Si0 + H2+O= Na2Si+4O3 + 2H20
Фтор окисляет щёлочи:
2F20 + 4NaO-2H = O20 + 4NaF— + 2H2O
Более подробно про эти реакции можно прочитать в статье Окислительно-восстановительные реакции.
8. Щёлочи не разлагаются при нагревании.
Исключение — гидроксид лития:
2LiOH = Li2O + H2O

Ошибки допускают окружающие, ошибки допускаем и мы сами. Тот, кто грамотно реагирует на ошибки свои, обычно более грамотно реагирует и на ошибки окружающих. Не так важно, с какого конца начинать учиться — важно, чтобы на любые ошибки, и свои и чужие, мы реагировали грамотно, то есть эффективно для дела и экологично для человека.
Первое, на что нужно обращать внимание — это то, что жизнь состоит не из одних ошибок. Да, человек рядом с вами сейчас совершил ошибку. Но в этот же момент он мог одновременно создать радость и совершить подвиг. Вокруг этого человека и вас было много других обстоятельств: вы точно решили, что нужно обращать внимание именно на эту ошибку и именно сейчас?
Может быть, вы разглядите, что (например) этот человек пробует, учится и старается. Может быть, вы вспомните и то, что этот человек — ваш любимый (такое бывает, да?) или заметите, что перед вами — красивый человек, и вы можете им любоваться даже тогда, когда он (или она) совершает ошибки…
Это не значит, что умные люди ошибки не замечают. Не замечают ошибки — люди безответственные, те, которым не приходится платить за последствия ошибок. Замечать нужно все. А на что обращать внимание свое или чужое — это вопрос уже другой. Ответственный человек внимательно относится к ошибкам, как своим, так и чужим. При этом, заметив ошибку, ответственный человек торопится думать, а не выдавать импульсивные негативные реакции, подбирает слова и интонации, время и место. Если же реагирование на ошибку идет сразу и тем более с превышением, это реакция не ответственного, а негативно настроенного человека, для которого ошибка — только хороший повод ударить другого человека.
Тем не менее, вопросы остаются: как оценить ошибку другого? Что это: мелочь или ужас-ужас-ужас? Случайно или намеренно? Мог предусмотреть или это нереально? — На эти вопросы каждый отвечает самостоятельно, и любопытно бывает посмотреть, кто ошибается в какую сторону. Злой и раздраженный человек отвечает сразу и определенно: «Мог предусмотреть! И вообще он сделал это — специально!», с ним солидаризуются все негативисты и невротики, при этом последние, как и человек-ребенок, любят видеть везде себе обиду, а негативисты вместо маленькой ошибки видит большой ужас. Человек, склонный все переживать — переживает, деятельная личность — думает как исправить. Недоброжелательно настроенный человек чаще склонен к наказанию за совершенные ошибки, доброжелательный — чаще склонен не заметить и простить. Человек в спокойном и позитивном состоянии духа обдумывает разные версии и рассматривает ситуацию с разных сторон.
Истории из жизни
Я слышу звук стартера, и машина за моей спиной начинает рывками уверенно двигаться вниз, прямо в овраг. За стеклом машины вижу застывшее от испуга лицо ребенка, до оврага – не больше 3 метров. Боком впрыгиваю-втискиваюсь в уезжающую из-под меня машину, выдергиваю ключи из замка зажигания…
Губарева Вера Александровна, г.Нижнекамск РТ
Муниципальное общеобразовательное учреждение
«Средняя общеобразовательная школа №7»
Г.Нижнекамск, Республика Татарстан
«Общие химические
свойства металлов»
Конспект урока для 9 класса
в сопровождении презентации
Выполнила
Учитель химии
Губарева Вера Александровна
Нижнекамск 2010
Урок по теме:
«Общие химические свойства металлов. Ряд активности».
Тип урока: урок изучения нового материала
Вид урока: мультимедийный
Цель урока: систематизировать сведения о химических свойствах металлов, рассмотренных при изучении материала курса химии 8,9 классов, выявить особенности протекания реакций металлов со сложными веществами, подчеркнуть химическую функцию металлов как восстановителей.
Задачи урока:
-
развивать умения пользоваться опорными знаниями, закреплять умения и навыки выполнения химического эксперимента;
-
развивать логическое мышление, умение анализировать увиденное;
-
закреплять умения составлять уравнения окислительно-восстановительных реакций;
-
сформировать понимание практического значения металлов в жизни человека;
-
Развивать познавательный интерес при выполнении теоретических и практических заданий.
Оборудование и реактивы:
на столах учащихся: раствор соляной кислоты (НCl), CuSO4 (раствор), металлы: цинк, медь, железо ( железные гвозди на ниточках), пробирки, штатив для пробирок, емкость для слива, спиртовка, щипцы, спички.
На столе учителя: предметный столик, спички, спиртовка, вата, шпатель, асбестовая прокладка, порошок магния, натрий, эксикатор с водой, фенол-фталеин.
Оснащение урока.
Компьютер, мультимедиапроектор, экран, таблицы « Растворимость кислот, солей и оснований в воде», « Периодическая система химических элементов Д.И.Менделеева», «Электрохимический ряд напряжений металлов», рабочие листы учащихся.
Ход урока:
I. Орг. момент (готовность учащихся к уроку) (1 мин.)
Сообщение темы урока слайд №1,2.
II. Проверка опорных знаний (10 мин.).
1. Вопросы классу:
-
По каким свойствам мы узнаём простые вещества металлы (слайд № 3).
-
Где находятся в ПСХЭ химические элементы металлы.
-
Является ли деление элементов на металлы и неметаллы условным?
Почему?
2. Программированный опрос
(учащимся предлагается тест из 5 вопросов (2 варианта)).
В тесте выделены ответы – верные и неверные.
Учащиеся записывают номера ответов в тетрадях.
« Самопроверка». слайд№4
Объявление результатов: 5 правильных ответов – «5»
4 правильных ответа – «4»
3 правильных ответа – «3»
III. Изучение нового материала. ( 27 мин.- 30 мин.)
Постановка цели урока. Актуальность изучения данной темы.
Учитель: Мир вокруг нас – это совокупность физических и химических превращений веществ. Как ведут себя металлы в этом мире, с какими веществами они взаимодействуют и каким должно быть их практическое применение. слайд№5
Почему одни металлы можно хранить в обычном состоянии, а другие либо в запаянном сосуде, либо под слоем керосина? слайд№6
Примечание: результат работы учащихся – конспект, включающий схему-опору по определённым свойствам металлов и уравнения реакций в качестве примера.
Химические свойства металлов делятся на две группы – с простыми веществами и сложными слайд№7
1) Взаимодействие металлов с простыми веществами. слайд№8
Вопрос: Как называются продукты взаимодействия металлов с кислородом, галогенами, серой, азотом (учащиеся дают ответы, сверяют их с записью на слайдах).
Техника безопасности
Лабораторный опыт №1. Прокаливание медной пластинки в пламени спиртовки. слайд№9
Наблюдения, уравнения реакций записывают в рабочем листе.
Демонстрационный опыт (видеоклип): горение магния в кислороде. слайд№9
Вопрос: Как вы можете объяснить этот опыт? Где подобный процесс мог применяться?
( В прошлом веке использовался фотографами для улучшения освещения)
Ученик у доски: Составляет уравнение реакции горения магния в кислороде, определяет окислитель и восстановитель.
Демонстрационный опыт (видеоклип): Взаимодействие сурьмы с хлором. слайд№10
Ученик у доски: Составляет уравнение реакции взаимодействия сурьмы с хлором, определяет окислитель и восстановитель.
Закрепление. Допишите уравнения реакций взаимодействия металлов с другими неметаллами. слайд№10, 11
Al + I2 →
Fe + S →
Na + N2 →
Ca + P →
Физкультпауза Выполняются упражнения для глаз.
2) Взаимодействие металлов с водой. слайд№12
Активные металлы(Li – Na) + вода → гидроксид металла(щелочь) + Н2↑
Металлы средней активности(Mg – Pb) + вода → оксид металла + Н2↑
Неактивные металлы (Bi – Au) + вода → не реагируют
«Как вы думаете ?»… имеет ли смысл фраза, которую мы часто слышим в сказках: «К морю синему пошли и море синее зажгли?».
слайд №13.
Демонстрационный опыт: «Активные металлы и вода».(видеоклип)
Ученик у доски: Составляет уравнения реакции взаимодействия натрия с водой. Фиксирует признаки химической реакции, определяет окислитель и восстановитель.
Закрепление. Допишите уравнения возможных реакций взаимодействия металлов водой. Слайд№14
Al + H2O →
Zn + H2O →
Ag + H2O →
Проблема: почему алюминий не реагирует с водой? Это свойство имеет практическое значение, т.к. для изготовления посуды не берут калий, натрий, а именно алюминий, цинк, железо.
3) Взаимодействие металлов с кислотами. слайд №15.
Лабораторный опыт №2. Взаимодействие цинка, железа, меди с соляной кислотой. ТБ
1 вариант — Zn + HCl
2 вариант — Cu + HCl
3 вариант – Fe + HCl
Учитель: контролирует правила ТБ при выполнении опытов, навыки и умения экспериментальной работы.
Запись в тетрадях уравнений реакций, наблюдения
Zn + HCl → ZnCl2 + H2
Fe + HCl → FeCl2 + H2
Cu + HCl → не идёт
Это свойство используется для получения водорода в лаборатории.
Объясните результаты опыта.
Вывод. Металлы , стоящие в ряду активности до водорода вытесняют его из растворов кислот, а после водорода — не вытесняют. . слайд №16
Но для этой реакции есть несколько поправок.
-
Если образуется растворимая соль;
-
Кроме щелочных и щелочно-земельных металлов;
-
Кроме концентрированной серной и азотной кислот.
-
Взаимодействие металлов с солями. слайд №17
Лабораторный опыт № 3. Взаимодействие железа с хлоридом меди и меди с хлоридом железа.
Учитель: контролирует правила ТБ при выполнении опытов, навыки и умения экспериментальной работы.
Запись в тетрадях уравнений реакций, наблюдения
Fe + CuCl2 → FeCl2 + Cu
FeCl2 + Cu → не идет
Для этой реакции тоже есть поправки, которые совпадают с первой и второй поправкой для кислот
Объясните результаты опыта.
Вывод. Более активные металлы вытесняют менее активные из растворов их солей.
Закрепление. Допишите уравнения возможных реакций. слайд №18
Ag + CuCl2 →
Zn + FeCl3 →
Fe + AgNO3 →
IV. Закрепление нового материала. слайд №19
-
Предлагается ребятам выполнить интерактивное упражнение:
С какими из веществ будут реагировать предложенные металлы при нормальных условиях? Выбрать правильные ответы.
-
Ответить на вопросы.
-
С какими веществами реагируют металлы?
-
Чем являются металлы в реакциях – окислителями или восстановителями?
-
Какие поправки вводятся для реакций металлов с водой, кислотами, солями?
-
Для чего нужно изучать химические свойства металлов? Где их можно использовать?
-
Где применить полученные знания?
Ответ: Металлы широко используются человеком в технике, медицине, различных отраслях промышленности, но при использовании надо учитывать их свойства: взаимодействие с кислородом, водой, различными солями.
V.Итоги урока. «Самооценка». Учащиеся оценивают свою работу на уроке по результатам теста и своим ответам. Учитель корректирует оценки и выставляет их в журнал.
VI. Домашнее задание.
-
Для всех: §8 , упр. 7,8 (письменно)
-
Придумать кроссворд по теме «Металлы»
Литература:
Химия. 9 класс: учеб. для общеобразоват.учреждений / О.С.Габриелян. – 14-е изд., испр. – М. : Дрофа, 2008
Использованные интернет – источники:
Слайд №6 взят из презентации Т.Я.Генераловой «Ряд напряжений металлов»
Анимационные картинки – http://tana.ucoz.ru/load/115-6-2
Видео опыты — http://www.alhimikov.net/video/neorganika/menu.html
Физкультпауза – интернет-источник неизвестен
Общие химические свойства металлов
Взаимодействие с неметаллами
Щелочные металлы сравнительно легко реагируют с кислородом, но каждый металл проявляет свою индивидуальность:
-
оксид образует только литий
4Li + O2 = 2Li2O
-
натрий образует пероксид
2Na + O2 = Na2O2
-
калий, рубидий и цезий — надпероксид
K + O2 = KO2
Остальные металлы с кислородом образуют оксиды:
2Mg + O2 = 2MgO
2Al + O2 = Al2O3
2Zn + O2 = 2ZnO (при нагревании)
4Cr + 3O2 = 2Cr2O3
Металлы, которые в ряду активности расположены левее водорода, при контакте с кислородом воздуха образуют ржавчину. Например, так делает железо:
4Fe + 3O2 (воздух) + 6H2O(влага) = 4Fe(OH)3
С галогенами металлы образуют галогениды:
2Na + Cl2 = 2NaCl
Mg + Cl2 = MgCl2
2Al + 3Br2 = 2AlBr3
Zn + Cl2 =ZnCl2
2Cr + 3Cl2 = 2CrCl3
Медный порошок реагирует с хлором и бромом (в эфире):
Cu + Cl2 = CuCl2
Cu + Br2 = CuBr2
При взаимодействии с водородом образуются гидриды:
2Na + H2 = 2NaH
Ca + H2 +СaH2
Zn + H2 =ZnH2
Взаимодействие с серой приводит к образованию сульфидов (реакции протекают при нагревании):
2K + S = K2S
Сa + S = CaS
2Al + 3S = Al2S3
2Cr + 3S = Cr2S3
Cu +S = CuS
Реакции с фосфором протекают до образования фосфидов (при нагревании):
3K + P = K3P
3Mg + 2P = Mg3P2
3Zn + 2P = Zn3P2
Основной продукт взаимодействия металла с углеродом — карбид (реакции протекают при нагревании).
Из щелочноземельных металлов с углеродом карбиды образуют литий и натрий:
2Li + 2C = Li2C2
Калий, рубидий и цезий карбиды не образуют, могут образовывать соединения включения с графитом:
Ca + 2C = CaC2
С азотом из металлов IA группы легко реагирует только литий. Реакция протекает при комнатной температуре с образованием нитрида лития:
6Li + N2 = 2Li3N
3Mg + N2 = Mg3N2
2Al + N2 = 2AlN
2Cr + N2 = 2CrN
Взаимодействие с водой
Все металлы I A и IIA группы реагируют с водой, в результате образуются растворимые основания и выделяется H2. Литий реагирует спокойно, держась на поверхности воды, натрий часто воспламеняется, а калий, рубидий и цезий реагируют со взрывом:
2Li + 2H2O = 2LiOH + H2
Ca + 2H2O = Ca(OH)2 + H2
Металлы средней активности реагируют с водой только при условии, что металл нагрет до высоких температур. Результат данной реакции — образование оксида.
Cr + H2O = Cr2O3 + H2
Zn + H2O = ZnO + H2
Неактивные металлы с водой не взаимодействуют.
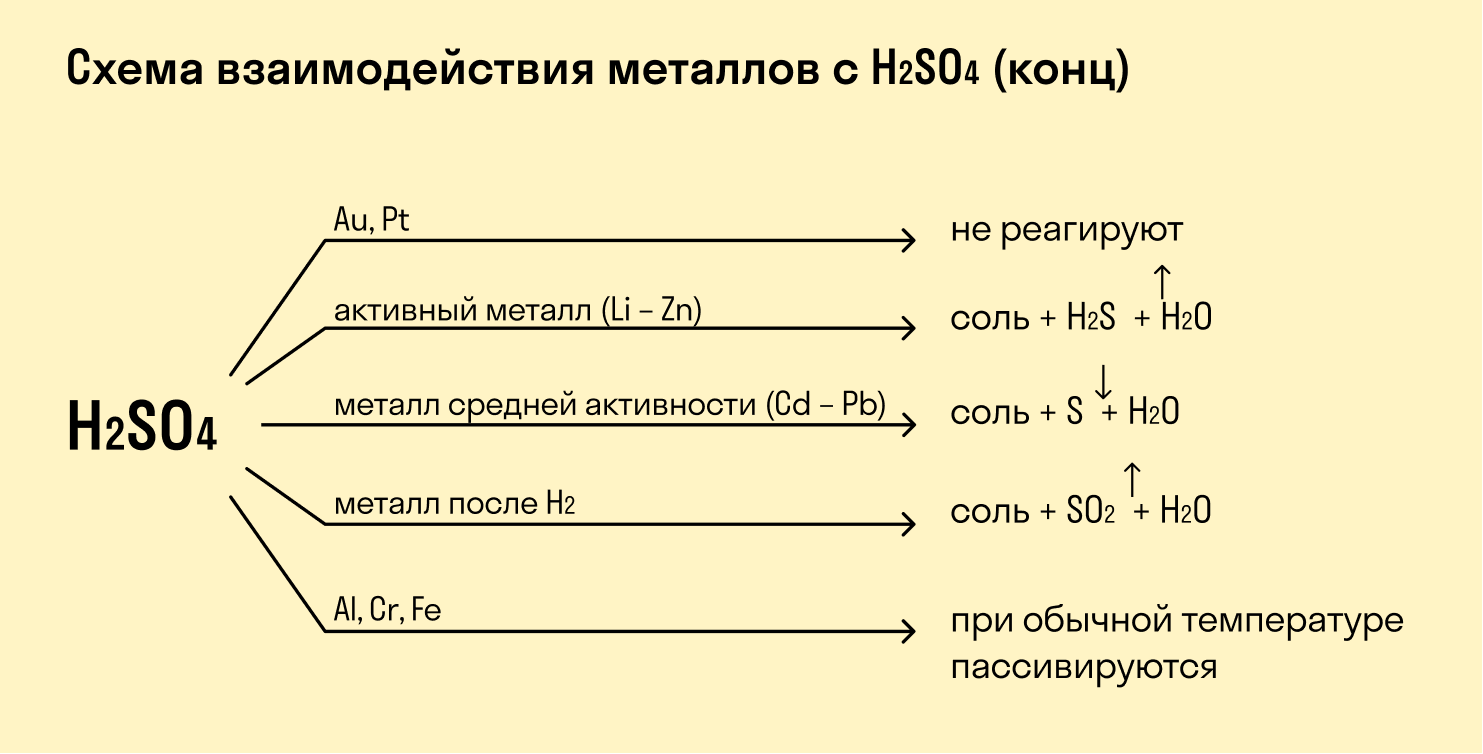
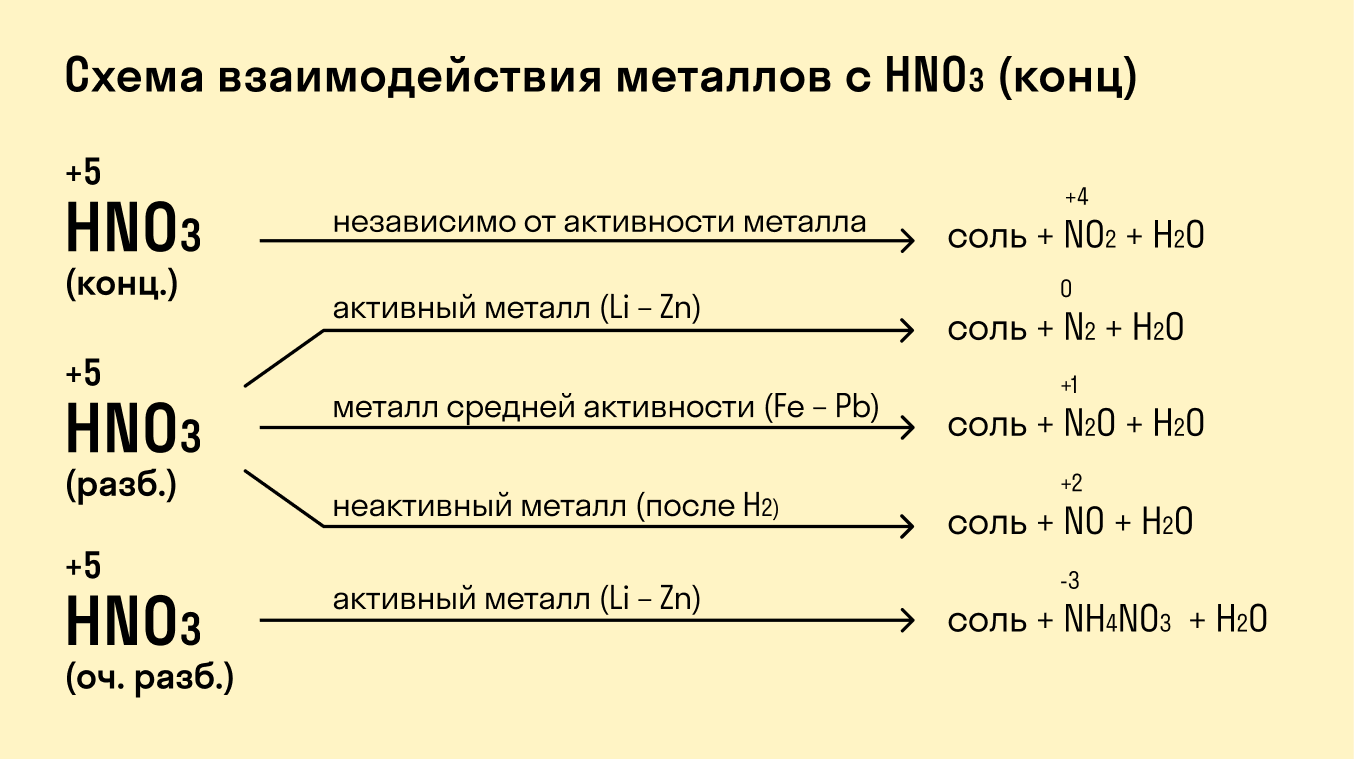
Взаимодействие с кислотами
Если металл расположен в ряду активности левее водорода, то происходит вытеснение водорода из разбавленных кислот. Данное правило работает в том случае, если в реакции с кислотой образуется растворимая соль.
2Na + 2HCl = 2NaCl + H2
При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно.
Металлы IА группы:
2K + H2SO4 (раствор) = K2SO4 + H2
8K + 5H2SO4 (конц) = 4K2SO4 + H2S + 4H2O
8Na + 10HNO3 (раствор) = 8NaNO3 + NH4NO3 + 3H2O
3Na + 4HNO3 (конц) = 3NaNO3 + NO + 2H2О
Металлы IIА группы
Mg + H2SO4 (раствор) = MgSO4 + H2
4Mg + 5H2SO4 (конц) = 4MgSO4 + H2S + 4H2O
Mg+ 4HNO3 (конц) = Mg(NO3)2 + 2NO2 + 2H2O
4Mg + 10HNO3 (раствор) = 4Mg(NO3)2 + 2N2O + 5H2O
Такие металлы, как железо, хром, никель, кобальт на холоде не взаимодействуют с серной кислотой, но при нагревании реакция возможна.
Взаимодействие с солями
Металлы способны вытеснять из растворов солей другие металлы, стоящие в ряду напряжений правее, и могут быть вытеснены металлами, расположенными левее:
Zn + CuSO4 = ZnSO4 + Cu
На металлы IА и IIА группы это правило не распространяется, так как они реагируют с водой.
Реакция между металлом и солью менее активного металла возможна в том случае, если соли — как вступающие в реакцию, так и образующиеся в результате — растворимы в воде.
Взаимодействие с аммиаком
Щелочные металлы реагируют с аммиаком с образованием амида натрия:
2Li + 2NH3 = 2LiNH2 + H2
Взаимодействие с органическими веществами
Металлы IА группы реагируют со спиртами и фенолами, которые проявляют в данном случае кислотные свойства:
2Na + 2C2H5OH = 2C2H5ONa + H2
2K + 2C6H5OH = 2C6H5OK + H2
Также они могут вступать в реакции с галогеналканами, галогенпроизводными аренов и другими органическими веществами.
Взаимодействие металлов с оксидами
Для металлов при высокой температуре характерно восстановление неметаллов или менее активных металлов из их оксидов.
8Al + 3Fe3O4 = 4Al2O3 + 9Fe (алюмотермия)
3Са + Cr2O3 = 3СаО + 2Cr (кальциетермия)
Получай лайфхаки, статьи, видео и чек-листы по обучению на почту
Узнай, какие профессии будущего тебе подойдут
Пройди тест — и мы покажем, кем ты можешь стать, а ещё пришлём подробный гайд, как реализовать себя уже сейчас
Вопросы для самоконтроля
-
С чем реагируют неактивные металлы?
-
С чем связаны восстановительные свойства металлов?
-
Верно ли утверждение, что щелочные и щелочноземельные металлы легко реагируют с водой, образуя щелочи?
-
Методом электронного баланса расставьте коэффициенты в уравнении реакции по схеме:
Mg + HNO3 → Mg(NO3)2 + NH4NO3 + Н2O
-
Как металлы реагируют с кислотами?
Подведем итоги
От активности металлов зависит их химические свойства. Простые вещества — металлы в окислительно-восстановительных реакциях являются восстановителями. По положению металла в электрохимическом ряду можно судить о том, насколько активно он способен вступать в химические реакции (т. е. насколько сильно у металла проявляются восстановительные свойства).
Напоследок поделимся таблицей, которая поможет запомнить, с чем реагируют металлы, и подготовиться к контрольной работе по химии.
Таблица «Химические свойства металлов»
Химические свойства оснований
1. Щелочи (растворимые основания) из металлов реагируют только с Zn, Be и Al:
Zn + 2NaOH + 2H2O → Na2[Zn(OH)4] + H2
Be + 2NaOH + 2H2O → Na2[Be(OH)4] + H2
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
Cr + NaOH → реакция не идет
Fe + NaOH → реакция не идет
2. Щелочи из неметаллов реагируют только с S, P, Si и галогенами:
3S + 6NaOH → Na2SO3 + 2Na2S + 3H2O
P4 + 3NaOH + 3H2O → PH3 + 3NaH2PO2 (t°, гипофосфит натрия)
Si + 2NaOH + H2O → Na2SiO3 + 2H2
Cl2 + 2NaOH → NaCl + NaClO + H2O (аналогично для Br2, I2)
3Cl2 + 6NaOH → 5NaCl + NaClO3 + 3H2O (при нагревании, аналогично для Br2, I2).
2F2 + 2NaOH → OF2 + 2NaF + H2O (продукты этой реакции на ЕГЭ не проверяются, но необходимо знать, что реакция протекает)
3. Основания взаимодействуют с кислотами с образованием средних, кислых или основных солей. Тип соли зависит от соотношения реагентов: например, в избытке кислоты образуются кислые соли.
Условие: один из реагентов должен быть растворимым.
H2SO4 + 2KOH → K2SO4 + 2H2O (соотношение реагентов 1:2)
H2SO4 + KOH → KHSO4 + H2O (соотношение реагентов 1:1)
HCl + Cu(OH)2 → CuOHCl + H2O или
2HCl + Cu(OH)2 → CuCl2 + 2H2O
H2SiO3 + Cu(OH)2 → реакция не идет, так как и H2SiO3 и Cu(OH)2 нерастворимые.
4. Основания взаимодействуют с солями
Условие: 1) оба реагента должны быть растворимыми; 2) должен выпадать осадок или выделяться газ.
2NaOH + ZnCl2 → Zn(OH)2
NaOH + NH4NO3 → NH3
Cu(OH)2 + NaNO3 → реакция не идет, так как гидроксид меди (II) нерастворим.
5. Основания реагируют с кислотными оксидами. Если оксид в избытке образуется кислая соль:
Ca(OH)2 + CO2 → CaCO3 + H2O
Ca(OH)2 + 2CO2 → Ca(HCO3)2
6. Щелочи реагируют с амфотерными оксидами:
1) реакции в растворе:
ZnO + 2NaOH + H2O → Na2[Zn(OH)4] (тетрагидроксоцинкат натрия)
BeO + 2NaOH + H2O → Na2[Be(OH)4] (тетрагидроксобериллат натрия)
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4] (тетрагидроксоалюминат натрия)
2) реакции при сплавлении:
ZnO + 2NaOH → Na2ZnO2 + H2O (цинкат натрия)
BeO + 2NaOH → Na2BeO2 + H2O (бериллат натрия)
Al2O3 + 2NaOH → 2NaAlO2 + H2O (метаалюминат натрия)
7. Щелочи реагируют с амфотерными гидроксидами:
1) реакции в растворе:
Zn(OH)2 + NaOH → Na2[Zn(OH)4]
Be(OH)2 + NaOH → Na2[Be(OH)4]
Al(OH)3 + NaOH → Na[Al(OH)4]
2) реакции при сплавлении:
Zn(OH)2 + 2NaOH → Na2ZnO2 + 2H2O (кислота: H2ZnO2)
Be(OH)2 + 2NaOH → Na2BeO2 + 2H2O (кислота: H2BeO2)
Al(OH)3 + NaOH → NaAlO2 + 2H2O (кислота: HAlO2)
8. Нерастворимые основания (а также Ca(OH)2 и LiOH) разлагаются при нагревании:
Ca(OH)2 → CaO + H2O
2LiOH → Li2O + H2O
Mg(OH)2 → MgO + H2O
Fe(OH)2 → FeO + H2O
Cu(OH)2 → CuO + H2O.